«`html
Геномные перестройки: новый подход к генетическим изменениям
Практические решения и ценность
Геномные перестройки играют важную роль в генетическом разнообразии, исследования показали, что мобильные генетические элементы (MGEs) могут использоваться для мобилизации ДНК, расширяя возможности за пределы традиционных методов, таких как CRISPR.
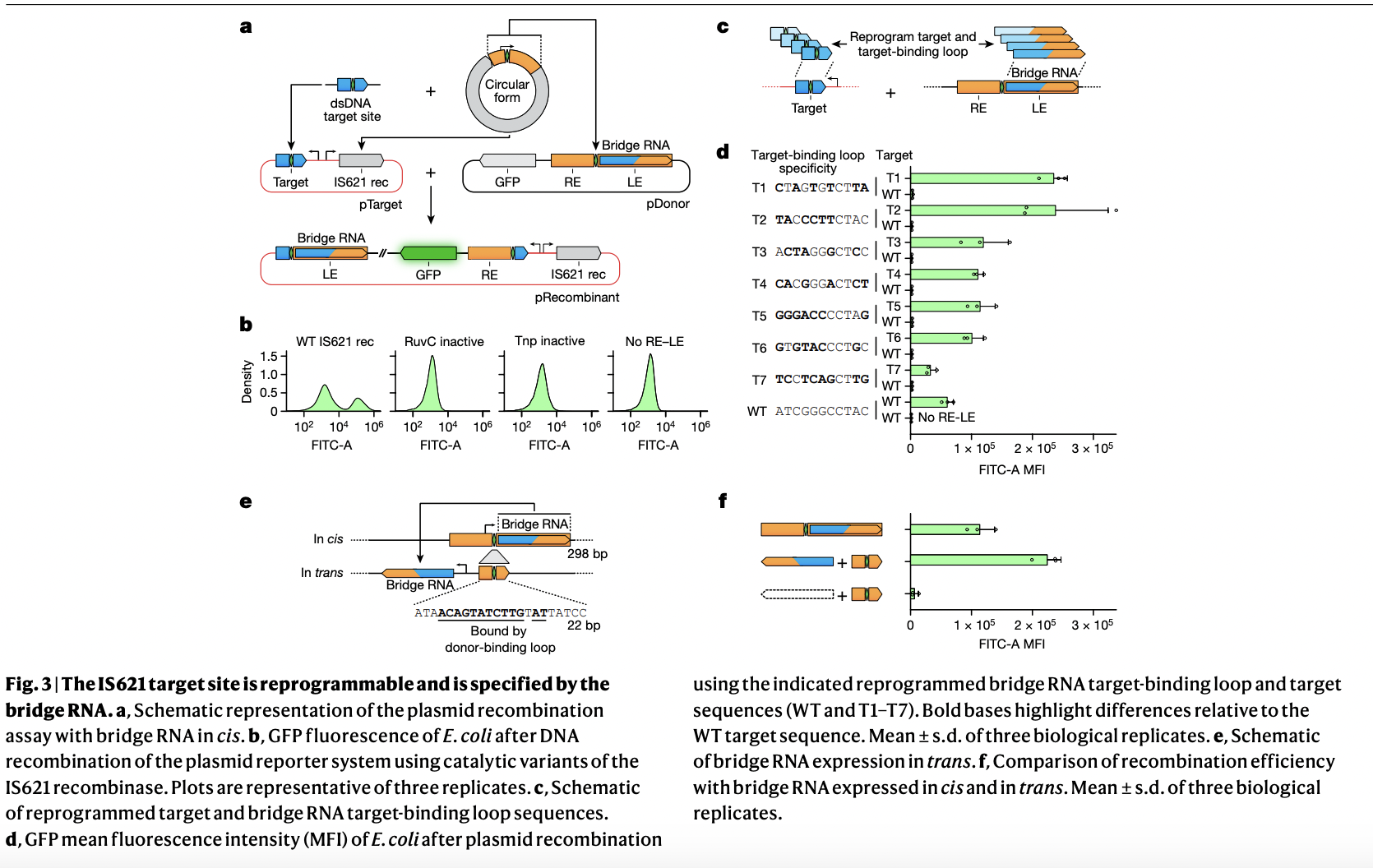
Исследователи обнаружили, что вставочные последовательности IS110 выражают структурированный не-кодирующий РНК, взаимодействующий с их рекомбиназой. Эта «мостовая» РНК имеет две петли, которые специфически связываются как с целевой ДНК, так и с донорной ДНК элемента IS110. Эти петли могут быть независимо перепрограммированы для облегчения последовательностно-специфической рекомбинации, позволяя вставке, эксцизии или инверсии ДНК-отрезков.
Исследования с использованием системы рекомбинации IS621 в *E. coli* показали ее высокую специфичность и программирование. Исследователи достигли целенаправленной рекомбинации с высокой точностью, используя настраиваемые мостовые РНК, которые точно соответствуют целевым последовательностям ДНК. Эта способность перепрограммирования мостовой РНК IS621 для точной целевой ДНК и вставки подчеркивает ее потенциал для точной генной инженерии с минимальными побочными эффектами.
Открытие мостовой РНК представляет собой новую парадигму в генетической манипуляции под руководством РНК, отличную от известных систем, таких как tRNA, CRISPR РНК и snoRNAs. В отличие от одноцепочечных РНК-гидов, мостовые РНК являются биспецифическими молекулами, которые оркестрируют точное выравнивание донорной и целевой последовательностей ДНК для эффективной рекомбинации.
Для получения дополнительной информации ознакомьтесь с статьей 1 и статьей 2. Вся заслуга за это исследование принадлежит ученым этого проекта. Также не забудьте подписаться на наш Twitter.
Присоединяйтесь к нашему каналу в Telegram и группе в LinkedIn.
Если вам нравится наша работа, вам понравится наш новостной бюллетень.
Не забудьте присоединиться к нашему сообществу в 45k+ ML SubReddit.
Исследование разработало обширную базу последовательностей из источников, таких как NCBI и MGnify, содержащую метагеномы, MAGs и вирусные геномы. Последовательности белков IS110 были аннотированы, сгруппированы и проанализированы на предмет сохраненных остатков и филогении.
Эксперименты с системой рекомбинации IS621 в *E. coli* продемонстрировали ее высокую специфичность и программирование. Исследователи достигли целенаправленной рекомбинации с значительной точностью, используя настраиваемые мостовые РНК, которые точно соответствуют целевым последовательностям ДНК. Система предпочитала точные совпадения, а толерантность к несовпадениям была низкой, что указывает на высокую достоверность.
В заключение, открытие мостовой РНК представляет собой новую парадигму в генетической манипуляции под руководством РНК, отличную от известных систем, таких как tRNA, CRISPR РНК и snoRNAs. Мостовые РНК являются биспецифическими молекулами, оркестрирующими точное выравнивание донорной и целевой последовательностей ДНК для эффективной рекомбинации.
Подробнее ознакомьтесь с статьей 1 и статьей 2. Вся заслуга за это исследование принадлежит ученым этого проекта. Также не забудьте подписаться на наш Twitter.
Присоединяйтесь к нашему каналу в Telegram и группе в LinkedIn.
Если вам нравится наша работа, вам понравится наш новостной бюллетень.
Не забудьте присоединиться к нашему сообществу в 45k+ ML SubReddit.
Для получения дополнительной информации ознакомьтесь с статьей 1 и статьей 2. Вся заслуга за это исследование принадлежит ученым этого проекта. Также не забудьте подписаться на наш Twitter.
Присоединяйтесь к нашему каналу в Telegram и группе в LinkedIn.
Если вам нравится наша работа, вам понравится наш новостной бюллетень.
Не забудьте присоединиться к нашему сообществу в 45k+ ML SubReddit.
Для получения дополнительной информации ознакомьтесь с статьей 1 и статьей 2. Вся заслуга за это исследование принадлежит ученым этого проекта. Также не забудьте подписаться на наш Twitter.
Присоединяйтесь к нашему каналу в Telegram и группе в LinkedIn.
Если вам нравится наша работа, вам понравится наш новостной бюллетень.
Не забудьте присоединиться к нашем сообществу в 45k+ ML SubReddit.
«`






















